Av: Dr Marco V. Benavides Sánchez.
Vid njurtransplantation kan en enda bild förändra en patients öde. En njurbiopsi är inte bara ett vävnadsprov: det är en mikroskopisk redogörelse för vad som händer i ett vitalt organ, ett fönster till hälsan hos ett transplantat eller en inhemsk njure. Det finns dock inneboende begränsningar för vår mest uppskattade diagnostiska metod: biopsi. Det mänskliga ögats subjektivitet, trötthet, anatomisk komplexitet och inter-observatörsvariabilitet har i åratal varit tysta hinder i vår kliniska praktik.
Men idag bevittnar vi en verklig tyst revolution. Artificiell intelligens (AI), ett verktyg som verkade avlägset för bara några år sedan, spränger nu in på området för njursjukdomar med kraft och elegans. Och det gör det inte för att ersätta oss, utan för att stödja oss, för att erbjuda oss större precision, konsekvens och nya diagnostiska möjligheter.
Komplexiteten av analys i njurbiopsier
Vi som har arbetat inom transplantationsområdet vet att en njurbiopsi kan avgöra om immunsuppression ska fortsätta eller avbrytas, behovet av intensifiering av behandlingen eller i värsta fall indikationen för transplantatnefrektomi. I detta sammanhang är diagnostisk precision avgörande.
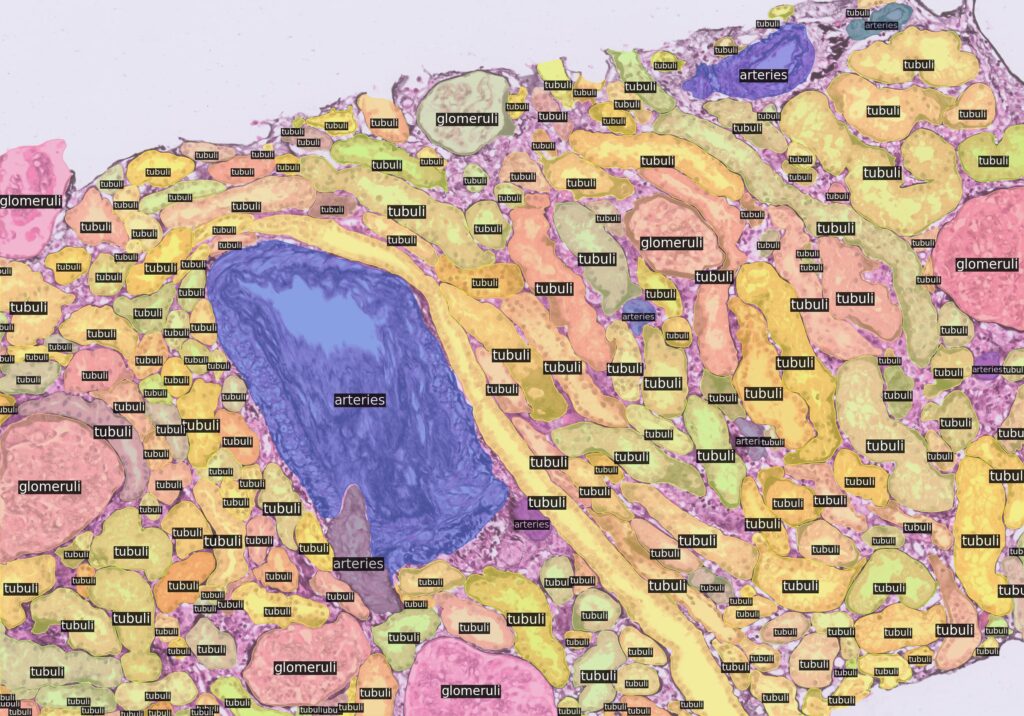
Njurpatologen måste möta ett komplext scenario: bilder fulla av tätt fördelade strukturer – glomeruli, tubuli, artärer – var och en med sina egna morfologiska egenskaper. Lesioner kan vara subtila eller uppenbara, isolerade eller överlappande. Ibland existerar akuta och kroniska lesioner samtidigt, andra gånger hittar vi flera patologier i samma glomerulus eller tubuli. Och som vi väl vet kräver klassificeringssystem – såsom Banff-klassificeringen för transplantation eller klassificeringen av diabetisk nefropati – en detaljerad och kvantitativ avläsning av varje lesion.
Det är här variabiliteten mellan observatörer blir ett verkligt problem. Det som för en patolog kan se ut som ”segmentell skleros” kan av en annan tolkas som ”lindrig mesangial förändring”. Denna tvetydighet, även om den är oundviklig i många fall, kan förändra avgörande terapeutiska beslut.
Artificiell intelligens kommer in på scenen
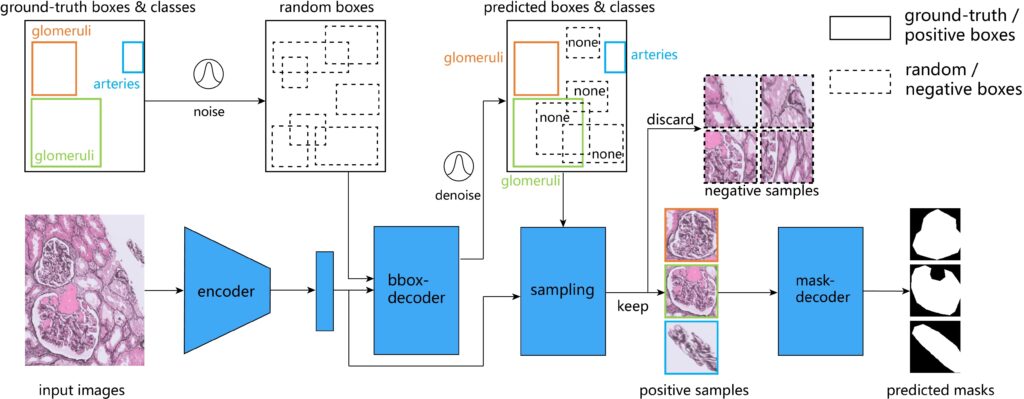
I detta sammanhang representerar studien som nyligen publicerades av Zhan Xiong och medarbetare i Artificial Intelligence in Medicine en störande milstolpe. Deras förslag: ett system som kallas DiffRegFormer, som kan utföra tät segmentering av anatomiska strukturer och klassificering av lesioner på njurbiopsibilder, med överraskande precision och anpassningsförmåga.
Det fascinerande med denna teknik är inte bara dess algoritmiska kraft, utan också dess design anpassad till de specifika utmaningarna med njurvävnad. Systemet kombinerar diffusionsmodeller, transformatorer och faltningsnätverk av RCNN-typ för att identifiera mer än 500 anatomiska strukturer i varje område av intresse. Glomeruli, tubuli och artärer segmenteras, känns igen och klassificeras automatiskt, utan behov av mänsklig inblandning.
Resultaten är lovande:
- 52,1 % genomsnittlig noggrannhet vid strukturdetektering.
- 46,8 % i anatomisk segmentering.
- 89,2 % noggrannhet i skadeklassificering.
- 64,6 % minns att identifiera specifika lesioner.
- Förmåga att överföra mellan färgningstekniker (Jones, PAS) utan omjustering eller omträning.
Dessa siffror är inte bara statistik. De är indikatorer på ett nytt paradigm: ett verktyg som kan minska felmarginalen, stödja patologen i komplexa diagnoser och framför allt ge konsekvens mellan institutioner.
Direkt applicering vid njurtransplantation
Ur ett transplantationsperspektiv är potentialen enorm. Överväg läsningen av en protokollbiopsi av transplantatet: uppenbarligen normala strukturer som, efter algoritmisk analys, avslöjar initiala mönster av kronisk skada eller subtila tecken på cellulär avstötning. Eller i biopsier baserade på en funktionell orsak, där AI skulle kunna underlätta objektiv identifiering och kvantifiering av interstitiell inflammation, vaskulit eller återkommande glomerulopatier.
Dessutom erbjuder AI ovärderligt stöd vid utbildning av nya patologer. Istället för att enbart förlita sig på det utbildade ögat från mer erfarna specialister kan invånarna lära sig i en stödjande miljö, där varje struktur är märkt, varje skada förklaras och varje mönster jämfört med en omfattande, validerad databas.
Påtagliga kliniska fördelar
- Minskning av interobservatörsvariabilitet: standardisering av diagnostiska kriterier mellan centra.
- Högre tolkningshastighet: idealisk för center med hög arbetsbelastning.
- Noggrann kvantifiering av lesioner: väsentligt i kliniska forskningsprotokoll.
- Stöd för medicinsk utbildning: strukturerad AI-baserad undervisning.
- Överföring mellan centra utan ytterligare kalibrering: större interoperabilitet mellan sjukhus.
Patologens expertöga är oersättlig. Men nu dyker det upp vid horisonten möjligheten att få stöd av ett verktyg som kombinerar precision, konsekvens och objektiv analys. Precis som stetoskopet förändrade medicinsk praxis på sin tid, omdefinierar artificiell intelligens vår förståelse av diagnos idag.
Synergin mellan det mänskliga sinnet och algoritmer kan leda oss till rättvisare, mer reproducerbar och datadriven medicin. Inom en snar framtid kan verktyg som DiffRegFormer rutinmässigt integreras i sjukhussystem, vilket gynnar både transplantationspatienten och specialisten som tar hand om dem.
Slutsats:
Vi står inför en ny era av medicin som involverar nefrologi i allmänhet och njurtransplantation i synnerhet. En där klinisk erfarenhet, patofysiologisk kunskap och medicinskt omdöme berikas av kraften hos artificiell intelligens. För varje mer exakt diagnos är en möjlighet att erbjuda effektivare behandling. Och varje verktyg som förbättrar vår precision är utan tvekan ytterligare ett hopp för våra patienter.
Hänvisning
Zhan Xiong, Junling He, Pieter Valkema, Tri Q. Nguyen, Maarten Naesens, Jesper Kers, Fons J. Verbeek. Advances in kidney biopsy lesion assessment through dense instance segmentation. Artificial Intelligence in Medicine. 2025. 103111. ISSN 0933-3657. https://doi.org/10.1016/j.artmed.2025.103111.
#ArtificialIntelligence #Medicine #Surgery #Medmultilingua


Lämna ett svar